近期,陈吉龙教授领衔的福建省畜禽病原感染与免疫学重点实验室先后在国际专业领域权威学术期刊Cell Reports、mBio等上发表流感等病毒感染与宿主免疫应答机理研究的最新成果。

流感病毒可引起畜禽等多种动物急性呼吸道疾病,不仅严重威胁着畜牧业生产,也是人类面临的最严重的公共卫生问题之一。此外,特定动物流感病毒也能突破物种间屏障造成人类感染,因此关于流感病毒的研究至关重要。陈吉龙教授团队研究发现在流感等病毒感染机体过程中,抗病毒信号通路的重要因子--STAT1的早期激活不依赖细胞因子和JAKs激酶,而Syk激酶发挥关键作用;该团队研究还表明,在流感等病毒感染过程中MIR155HG基因通过编码lncRNR-155和miRNA-155-5p在抗病毒免疫应答中发挥双重调控作用。这些成果发表在国际专业领域权威学术期刊mBio (Rai et al., 2022, 13(6):e0251022. doi: 10.1128/mbio.02510-22)、Journal of Virology (Li et al., 2022, 96(7):e0020022. doi: 10.1128/jvi.00200-22)上。
在上述研究基础上,近日陈吉龙教授团队揭示了在流感等病毒感染宿主的早期阶段,STAT3的激活不依赖于白细胞介素-6(IL-6),而依赖RIG-I/MAVS/Syk通路的新机制。此外,STAT3的早期激活参与调控多种抗病毒基因的表达。应用动物模型研究发现,与野生型小鼠相比STAT3Y705F/+小鼠在感染流感病毒后表现出更严重的病理损伤。STAT3 Y705F突变显著上调了I型、III型IFNs的表达。进一步应用构建的IFNAR1-/-STAT3Y705F/+小鼠和IFNLR1-/-STAT3Y705F/+小鼠模型进行深入研究,结果表明STAT3 Y705位点的磷酸化能够抑制过量的I型和III型IFNs的信号转导,从而维持机体正常的抗病毒免疫水平,避免过度免疫引起的器官损伤。这些发现有助于阐明病毒与宿主免疫系统之间复杂的互作机理,并为抗病毒药物设计提供潜在的靶点。
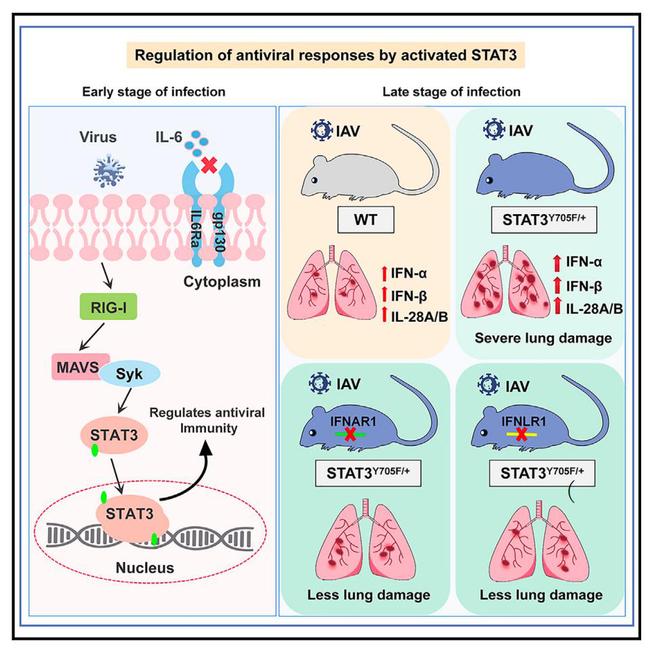
相关成果已在Cell Reports期刊上发表,题为“STAT3 regulates antiviral immunity by suppressing excessive interferon signaling”(Liu et al., 2023, 42(7):112806. doi: 10.1016/j.celrep.2023.112806)。陈吉龙教授为该论文的通讯作者,刘莎莎副教授、硕士生刘思亚和於子鼎为论文共同第一作者,乐鱼(中国)为第一完成单位。该项研究得到了国家重点研发计划项目(2021YFD1800205)和国家自然科学基金重点项目(32030110)的资助。
原文链接:https://doi.org/10.1016/j.celrep.2023.112806
